Cellule staminali e fattori di crescita
L’angiogenesi terapeutica rappresenta una delle più rilevanti acquisizioni della ricerca vascolare moderna, finalizzata allo sviluppo di nuove strategie di trattamento dell’ischemia critica degli arti inferiori, in particolare nei pazienti non candidabili a procedure di rivascolarizzazione chirurgica o endovascolare, o già sottoposti a tali interventi con esito insoddisfacente e ad alto rischio di amputazione arto inferiore
L’angiogenesi terapeutica è una terapia rigenerativa volta a stimolare la formazione di nuovi vasi sanguigni, con l’obiettivo di incrementare la perfusione ematica in territori ischemici, scarsamente vascolarizzati e ad alto rischio di lesioni trofiche, ulcerazioni e necrosi nella cura della ischemia critica non operabile
Questa metodica trova indicazione soprattutto negli stadi avanzati dell’arteriopatia obliterante periferica di origine aterosclerotica o diabetica, in pazienti affetti da ischemia critica degli arti inferiori, quadro clinico caratterizzato da:
- claudicatio intermittens con autonomia di marcia estremamente ridotta,
- dolore ischemico a riposo, spesso notturno,
- cute fredda e distrofica,
- ulcere cutanee (es. piede diabetico),
- lesioni necrotico-gangrenose (IV stadio di Fontaine).
Incremento del flusso e circolo collaterale
Come già descritto nel trattamento locoregionale dell’ischemia critica, un incremento efficace del flusso ematico nell’arto può essere ottenuto attraverso il potenziamento del circolo collaterale, che agisce come un bypass naturale in grado di superare le ostruzioni arteriose aterosclerotiche.
In presenza di un circolo collaterale adeguato, è possibile osservare:
- riduzione o risoluzione del dolore ischemico,
- recupero trofico dei tessuti,
- guarigione di ulcere cutanee anche complesse (Figura 1).
Al contrario, un circolo collaterale povero o assente, associato a un danno esteso del microcircolo capillare, rappresenta una condizione di particolare gravità, nella quale le terapie convenzionali risultano spesso inefficaci. In tali casi, il ricorso all’angiogenesi terapeutica può offrire risultati clinici promettenti.
Angiogenesi terapeutica: introduzione
L’angiogenesi è un processo fisiologico fondamentale, responsabile della formazione di nuovi vasi sanguigni durante lo sviluppo embrionale e nei meccanismi di riparazione dei tessuti danneggiati da traumi o patologie degenerative.
La capacità angiogenetica dell’organismo condiziona in modo determinante la guarigione di molte patologie ischemiche. L’angiogenesi terapeutica rappresenta una terapia rigenerativa vascolare con concrete opportunità nel trattamento dei casi più gravi di ischemia critica degli arti inferiori, patologia che, se trattata con metodiche convenzionali, presenta ancora oggi un rischio di amputazione maggiore fino al 50% (1).
Indicazioni cliniche
Le indicazioni cliniche al trattamento di angiogenesi terapeutica hanno riguardato prevalentemente:
- piede diabetico ischemico
- arteriopatia obliterante periferica
- gangrena ischemica del piede
in Pazienti già sottoposti a procedure di rivascolarizzazione periferica convenzionale (angioplastica + stent o bypass) risultate inefficaci per scarsità di letto periferico distale (run-off).
Caso clinico 1: F.L. 86 anni.
- A: estesa ulcera del calcagno in paziente con ischemia critica arto inferiore destro
- B: dopo debridement a ultrasuoni con esposizione dell’osso calcaneale
- C: 32° giorno dall’inizio della terapia con trattamento locoregionale vasoattivo e angiogenesi terapeutica
- D: 75° giorno
- E: completa guarigione al 105° giorno
Caso clinico 2: C.E. 65 anni.
Paziente con gangrena su base aterosclerotica del piede destro, già sottoposto a:
- due rivascolarizzazioni endovascolari (angioplastica + stent),
- amputazione del I dito.
- A–B: quadro lesionale iniziale con indicazione esterna ad amputazione di coscia
- C–D: 3° mese di trattamento con terapia locoregionale vasoattiva, disarticolazione del II e III dito, debridement a ultrasuoni e membrane collageniche
- E–F: 4°–5° mese
- G–H: avanzata guarigione al 6° e 9° mese
- I: completa risoluzione all’11° mese
Caso clinico 3: P.A. 55 anni.
Ischemia critica su base aterosclerotica dell’arto inferiore destro con necrosi del I, II e V dito.
- A: prima osservazione dopo trombolisi loco-regionale inefficace, non candidabile a PTA o bypass
- B: 46° giorno, arresto della progressione e recupero trofico
- C: 50° giorno
- D–E: 4° mese, rigenerazione tessutale
- F: 6° mese, completa rigenerazione e autoamputazione della falange distale del V dito
Caso clinico 4: S.E. 78 anni.
Paziente con ischemia critica arto inferiore sinistro, già amputato di coscia a destra.
- A–B–F: necrosi del I dito e ulcera cutanea di gamba
- G: dopo debridement a ultrasuoni
- C–H: 2° mese
- D–I: 3° mese e mezzo
- E–L: completa guarigione a 5 mesi e mezzo
Meccanismi biologici dell’angiogenesi
Con il termine angiogenesi si comprendono tre processi integrati:
- Angiogenesi propriamente detta: formazione di nuovi capillari da vasi preesistenti (Figura 1), indotta da ipossia e mediata da HIF-1 e VEGF fattori di crescita vascolare farmacologici
- Vasculogenesi: formazione di nuovi vasi a partire da cellule progenitrici endoteliali (EPCs, CD34+)
- Arteriogenesi: sviluppo e maturazione del circolo collaterale a partire da arteriole preesistenti, stimolata prevalentemente da fattori infiammatori (MCP-1) e shear stress
- Neoangiogenesi: formazione di nuovi capillari da vasi preesistenti a seguito di somministrazione di fattori di crescita vascolare farmacologici
Fattori di crescita e angiogenesi terapeutica
Fattori di crescita
Numerosi fattori di crescita (VEGF, FGF, eritropoietina) e cellule staminali CD34+ hanno dimostrato capacità angiogenetica, vasculogenetica e arteriogenetica in modelli sperimentali e clinici (Figura 2).
L’angiogenesi terapeutica forma terapeuticamente guidata di neoangiogenesi, favorendo l’aumento e distribuzione del circolo collaterale arterioso, rappresenta uno dei principali determinanti dell’incremento del flusso ematico periferico, risultando emodinamicamente più efficace rispetto al circolo collaterale preesistente nel Paziente arteriopatico (legge di Poiseuille)colpito da ischemia critica.
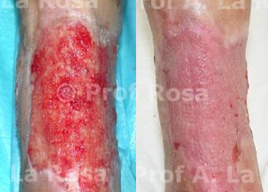
Pz.te di 78 anni portatrice di ulcera mista sulla faccia anteriore, A1 e laterale A2 di gamba SX con esposizione del tendine tibiale anteriore e peroneo lungo. Sottoposta a trattamento vasoattivo locoregionale e a metodo integrato, dopo 30 giorni dall’inizio della terapia si osserva in B discreta copertura dei tendini da parte del tessuto di granulazione. In C dopo 5 mesi di terapia; in D dopo 6 mesi di terapia; E, al 7° mese; completa guarigione al giorno 277°giorno di terapia F;ad un controllo dopo 2 mesi dalla guarigione G.
Cellule staminali e neovascolarizzazione
Le cellule progenitrici endoteliali derivate dal midollo osseo (CD34+) sono in grado di:
- favorire la neovascolarizzazione o neoangiogenesi
- rinforzare l’angiogenesi attraverso la secrezione di VEGF e FGF-2,
- contribuire alla riparazione della rete vascolare danneggiata.
La metodica più utilizzata prevede il prelievo di cellule dal midollo osseo della cresta iliaca e la loro somministrazione diretta nei territori ischemici.

Pz.te di 62 anni portatore di voluminosa e profonda lesione ulcerativa plantare SX in Pz.te con occlusione estesa della a. femorale superficiale SX, diabete mellito e frattura spontanea scomposta del tallone (A). Sottoposto ad intervento chirurgico di osteosintesi calcaneare, viene confezionata una finestra sul gesso applicato, al fine di poter procedere alla terapia rigenerativa sui tessuti della ferita (B). La terapia applicata ha contemplato : Metodo Integrato ( terapia con membrane collageniche + antibiotico terapia locale con catetere) più terapia vasoattiva locoregionale. C-D rispettivamente al 5° e 7° mese ti terapia) ; E, al 11° mese di trattamento; F al 14° mese; G, a completa chiusura della lesione, ottenuta al 16° mese di terapia. Pz.te di 62 anni portatore di v Voluminosa e profonda lesione ulcerativa plantare SX in Pz.te con occlusione estesa della a. femorale superficiale SX, diabete mellito e frattura spontanea scomposta del tallone (A). Sottoposto ad intervento chirurgico di osteosintesi calcaneare, viene confezionata una finestra sul gesso applicato, al fine di poter procedere alla terapia rigenerativa sui tessuti della ferita (B). La terapia applicata ha contemplato : Metodo Integrato ( terapia con membrane collageniche + antibiotico terapia locale con catetere) più terapia vasoattiva locoregionale. C-D rispettivamente al 5° e 7° mese ti terapia) ; E, al 11° mese di trattamento; F al 14° mese; G, a completa chiusura della lesione, ottenuta al 16° mese di terapia.
Terapia farmacologica locoregionale con fattori di crescita
Metodica
I fattori di crescita vengono somministrati al Paziente con la stessa metodica utilizzata nel salvataggio d’arto con terapia vasoattiva locoregionale.
Utilizzando la tecnica di Hannington-Kiff o via venosa reflua, già descritta, dopo svuotamento venoso e posizionamento del tourniquet per il blocco venoso ed arterioso locoregionale:
- si somministra la soluzione farmacologica tramite vena superficiale,
- il blocco circolatorio viene mantenuto per circa 18 minuti,
- manovre compressive favoriscono la distribuzione omogenea del farmaco.
Un buon risultato angiogenetico richiede che i Pz. vengano sottoposti a trattamento combinato vasoattivo e fattori di crescita precocemente, con richiami periodici di 2-3 mesi, fino a stabile incremento della perfusione periferica e stabilizzazione delle lesioni ischemiche.
Angiogenesi terapeutica: esperienza personale
Nella mia esperienza clinica svolta a Pavia, l’angiogenesi terapeutica viene impiegata nel trattamento di pazienti affetti da ischemia critica:
- non candidabili a rivascolarizzazione convenzionale,
- già sottoposti a interventi falliti,
- con o senza lesioni trofiche iniziali.
La metodica è sempre associata al trattamento vasoattivo locoregionale, che consente una rapida riduzione del dolore ischemico e un miglioramento della perfusione.
L’angiogenesi terapeutica agisce attraverso due meccanismi principali:
- Effetto protettivo immediato sui tessuti ischemici, con inibizione dell’apoptosi e riduzione dell’estensione necrotica fino al 50%
- Effetto angiogenetico tardivo, con sviluppo di nuovi capillari e miglioramento stabile della perfusione
L’azione combinata delle due terapie consente di ottenere maggiore efficacia nel:
- prevenire l’insorgenza di nuove lesioni ischemiche,
- arrestare la progressione della necrosi,
- ischemia critica non operabile
- ridurre significativamente il rischio di amputazione maggiore,
- favorire il salvataggio dell’arto ischemico anche in casi complessi.
Conclusioni
L’ischemia critica degli arti inferiori rappresenta lo stadio più avanzato e severo dell’arteriopatia ostruttiva periferica ed è gravata da un elevato rischio di amputazione e perdita funzionale dell’arto. Nei Pazienti non candidabili a procedure di rivascolarizzazione chirurgica o endovascolare, l’angiogenesi terapeutica associata alla terapia vasoattiva locoregionale costituisce un’opzione efficace per il salvataggio degli arti ischemici.
Attraverso la stimolazione della neoformazione vascolare e il miglioramento del microcircolo periferico, tale approccio consente una significativa riduzione del dolore ischemico a riposo, di migliorare la perfusione del microcircolo, favorire la guarigione delle lesioni ulcerative o destinate alla necrosi e preservare la funzionalità dell’arto, anche in quadri clinici complessi e avanzati. L’esperienza clinica documentata dimostra come, in una percentuale significativa di casi destinati all’amputazione, sia possibile ottenere stabilizzazione della malattia e recupero trofico dei tessuti.
In conclusione, l’angiogenesi terapeutica nell’ischemia critica degli arti inferiori rappresenta una strategia avanzata e mirata di cura, da integrare in un percorso diagnostico-terapeutico personalizzato, orientato al salvataggio dell’arto, alla riduzione delle amputazioni e al miglioramento della qualità di vita del Paziente.
Bibliografia
1. Norgren L, Hiatt WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FG, Bell K, Caporusso J, Durand-Zaleski I, Komori K, Lammer J, Liapis C, Novo S, Razavi M, Robbs J, Schaper N,
Shigematsu H, Sapoval M, White C, White J. Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II). Eur J Vasc Endovasc Surg. 2007;33 Suppl 1:S1-75.
2. Tateishi-Yuyama E, Matsubara H, Murohara T, Ikeda U, Shintani S, Masaki H, Amano K, Kishimoto Y, Yoshimoto K, Akashi H, Shimada K, Iwasaka T, Imaizumi T. Therapeutic angiogenesis for patients with limb ischemia by autologous transplantation of bone-marrow cells: a pilot study and a randomised controlled trial. Lancet. 2002;360:427-435.
3. Miyamoto M, Yasutake M, Takano H, Takagi H, Takagi G, Mizuno H, Kumita S, Takano T. Therapeutic angiogenesis by autologous bone marrow cell implantation for refractory chronic peripheral arterial disease using assessment of neovascularization by 99mTc-tetrofosmin (TF) perfusion scintigraphy. Cell Transplant. 2004;13:429-437.
4. Saito Y, Sasaki K, Katsuda Y, Murohara T, Takeshita Y, Okazaki T, Arima K, Katsuki Y, Shintani S, Shimada T, Akashi H, Ikeda H, Imaizumi T. Effect of autologous bone-marrow cell transplantation on ischemic ulcer in patients with Buerger’s disease. Circ J. 2007;71:1187-1192.
5. Takeshita S, Zheng LP, Brogi E, Kearney M, Pu LQ, Bunting S, Ferrara N, Symes JF, Isner JM. Therapeutic angiogenesis. A single intraarterial bolus of vascular endothelial growth factor augments revascularization in a rabbit ischemic hind limb model. J Clin Invest. 1994;93:662-670.
6. Van Weel V, Deckers MM, Grimbergen JM, van Leuven KJ, Lardenoye JH, Schlingemann RO, Nieuw Amerongen GP, van Bockel JH, van Hinsbergh VW, Quax PH. Vascular endothelial growth factor overexpression in ischemic skeletal muscle enhances myoglobin expression in vivo. Circ Res. 2004;95:58-66.
7. Rissanen TT, Markkanen JE, Gruchala M, Heikura T, Puranen A, Kettunen MI, Kholova I, Kauppinen RA, Achen MG, Stacker SA, Alitalo K, Yla-Herttuala S. VEGF-D is the strongest angiogenic and lymphangiogenic effector among VEGFs delivered into skeletal muscle via adenoviruses. Circ Res. 2003;92:1098-1106.
8. Hiasa K, Ishibashi M, Ohtani K, Inoue S, Zhao Q, Kitamoto S, Sata M, Ichiki T, Takeshita A, Egashira K. Gene transfer of stromal cell-derived factor-1alpha enhances ischemic vasculogenesis and angiogenesis via vascular endothelial growth factor/endothelial nitric oxide synthase-related pathway: next-generation chemokine therapy for therapeutic neovascularization. Circulation. 2004;109:2454-2461.
9. Asahara T, Bauters C, Zheng LP, Takeshita S, Bunting S, Ferrara N, Symes JF, Isner JM. Synergistic effect of vascular endothelial growth factor and basic fibroblast growth factor on angiogenesis in vivo. Circulation. 1995;92:II365-II371.
10. Shyu KG, Manor O, Magner M, Yancopoulos GD, Isner JM. Direct intramuscular injection of plasmid DNA encoding angiopoietin-1 but not angiopoietin-2 augments revascularization in the rabbit ischemic hindlimb. Circulation. 1998;98:2081-2087.
11. Taniyama Y, Morishita R, Aoki M, Nakagami H, Yamamoto K, Yamazaki K, Matsumoto K, Nakamura T, Kaneda Y, Ogihara T. Therapeutic angiogenesis induced by human hepatocyte growth factor gene in rat and rabbit hindlimb ischemia models: preclinical study for treatment of peripheral arterial disease. Gene Ther. 2001;8:181-189.
12. Rabinovsky ED, Draghia-Akli R. Insulin-like growth factor I plasmid therapy promotes in vivo angiogenesis. Mol Ther. 2004;9:46-55.
13. Ozawa T, Toba K, Kato K, Minagawa S, Saigawa T, Hanawa H, Makiyama Y, Moriyama M, Honma KI, Isoda M, Hasegawa G, Naito M, Takahashi M, Aizawa Y. Erythroid cells play essential roles in angiogenesis by bone marrow cell implantation. J Mol Cell Cardiol. 2006;40:629-638.
14. Vincent KA, Shyu KG, Luo Y, Magner M, Tio RA, Jiang C, Goldberg MA, Akita GY, Gregory RJ, Isner JM. Angiogenesis is induced in a rabbit model of hindlimb ischemia by naked DNA encoding an HIF-1alpha/VP16 hybrid transcription factor. Circulation. 2000;102:2255-2261.
15. Khachigian LM. Early growth response-1 in cardiovascular pathobiology. Circ Res. 2006;98:186-191.
16. Hong KH, Ryu J, Han KH. Monocyte chemoattractant protein-1-induced angiogenesis is mediated by vascular endothelial growth factor-A. Blood. 2005;105:1405-1407.
17.Masataka S. Role of circulating vascular progenitors in angiogenesis, vascular healing, and pulmonary hypertension. Arteriosclerosis, Trombosis and Vascular Biology. 2006;26:1008.
18. Yousuke k, Yoshiaki T, Ken A, Yutaka S, Ken-ichiro S, Shinichi S, Toyoaki Murohara, Tsutomu I. Effect of bone marrow transplantation in patients with critical limb ischemia.Cardiovascular regeneration therapies using tissue engineering approaches( Book). Springer Tokio- 2005; 5:213-220.
19. Baumgartner I, Pieczek A, Manor O, Blair R, Kearney M, Walsh K, Isner JM. Constitutive expression of phVEGF165 after intramuscular gene transfer promotes collateral vessel
development in patients with critical limb ischemia. Circulation. 1998;97:1114-1123.
20. Kim HJ, Jang SY, Park JI, Byun J, Kim DI, Do YS, Kim JM, Kim S, Kim BM, Kim WB, Kim DK. Vascular endothelial growth factor-induced angiogenic gene therapy in patients with peripheral artery disease. Exp Mol Med. 2004;36:336-344.
21. Morishita R, Aoki M, Hashiya N, Makino H, Yamasaki K, Azuma J, Sawa Y, Matsuda H, Kaneda Y,Ogihara T. Safety evaluation of clinical gene therapy using hepatocyte growth factor to treat peripheral arterial disease. Hypertension. 2004;44:203-209.
22. Kusumanto YH, van Weel V, Mulder NH, Smit AJ, van den Dungen JJ, Hooymans JM, Sluiter WJ,Tio RA, Quax PH, Gans RO, Dullaart RP, Hospers GA. Treatment with intramuscular vascular endothelial growth factor gene compared with placebo for patients with diabetes mellitus and critical limb ischemia: a double-blind randomized trial. Hum Gene Ther. 2006;17:683-691.
23. Kipshidze N, Kipiani K, Beridze N, Roubin G, Tsapenko M, Shehzad MZ, Moses J, Kipshidze NN.Therapeutic angiogenesis for patients with limb ischemia by utilization of fibrin meshwork. Pilot randomized controlled study. Int Angiol. 2003;22:349-355.
24. Tateishi-Yuyama E, Matsubara H, Murohara T, Ikeda U, Shintani S, Masaki H, Amano K, Kishimoto Y, Yoshimoto K, Akashi H, Shimada K, Iwasaka T, Imaizumi T. Therapeutic
angiogenesis for patients with limb ischemia by autologous transplantation of bone-marrow cells: a pilot study and a randomised controlled trial. Lancet. 2002;360:427-435.
25. Bartsch T, Brehm M, Zeus T, Strauer BE. Autologous mononuclear stem cell transplantation in patients with peripheral occlusive arterial disease. J Cardiovasc Nurs. 2006;21:430-432.
26. Kajiguchi M, Kondo T, Izawa H, Kobayashi M, Yamamoto K, Shintani S, Numaguchi Y, Naoe T,Takamatsu J, Komori K, Murohara T. Safety and efficacy of autologous progenitor cell transplantation for therapeutic angiogenesis in patients with critical limb ischemia. Circ J. 2007;71:196-201.
27. K Nayan S Rao, Azan S Brinbrek, Burton E Sobel. Heart disease and erythropoietin. Future Cardiol. 2008; 4(1):57-64.
28. Parsa CJ, Matsumoto A, Kim J Riel RU, Pascal LS, Walton GB, Thompson RB, Petrofski JA, Annex BH, StamlerJS, Koch WJ. A novel protective effect of erythropoietin in the infracted heart. J Clin Invest 112:999-1007,2003.